
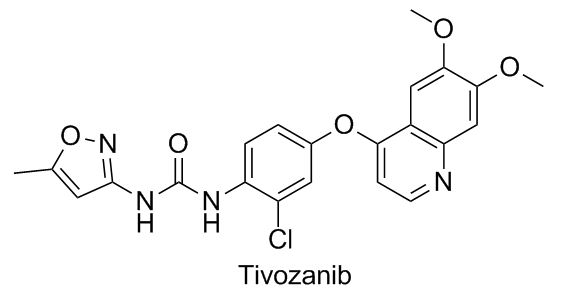
Tivozanib(VEGFR抑制剂)是口服VEGF受体酪氨酸激酶抑制剂。它已经完成了第一阶段的调查,用于治疗一线(治疗初治)肾细胞癌患者。Tivozanib于2017年8月获得欧洲药品管理局(EMA)的批准上市,又与近日被美国FDA批准。Tivozanib以盐酸盐一水合物的形式使用,其为白色至浅棕色粉末。它几乎不溶于水,在酸、乙醇和甲醇水溶液中溶解度低。它不吸湿,不具有光学活性。Tivozanib是甲喹啉脲衍生物,它能通过对被选择性地抑制血管内皮生长因子来抑制血管生成。
它由AVEO Pharmaceuticals开发。它被设计用于抑制所有三种VEGF受体。口服tivozanib后,2至24小时后达到最高血清水平。总AUC与食物摄入无关。当在血液中时,超过99%的物质与血浆蛋白结合,主要是白蛋白。尽管酶CYP3A4和CYP1A1以及几种UGT能够代谢药物,但超过90%以不变的形式循环。代谢物是去甲基化,羟基化和N-氧化产物和葡糖苷酸。
生物半衰期为4.5至5.1天;79%通过粪便排泄,大部分未改变,12%通过尿液排出,完全没有变化。使用利福平(CYP3A4酶的强诱导剂)施用单剂量的tivozanib,将tivozanib的生物半衰期和总暴露量(AUC)减少一半,但对血液中的最高浓度没有相关影响。与强效CYP3A4抑制剂酮康唑组合,没有相关的作用。这些发现的临床意义尚不清楚。最常见的副作用是高血压(高血压,48%的患者),发声障碍(声音嘶哑,27%),疲劳和腹泻(均为26%)。一个高血压危象的发生率为1%。
Tivozanib (VEGFR抑制剂)可用于研究Tivozanib抑制ABCB1和ABCG2介导的肿瘤细胞多药耐药。
ABC(ATP-binding cassette)跨膜转运蛋白超家族在肿瘤的耐药过程中起着很大的作用,影响着肿瘤细胞对不同药物的吸收、分布、代谢和排出。这些ABC跨膜转运蛋白超家族在肿瘤细胞常常高表达,与抗癌药物相结合,利用ATP水解释放能量促使药物被泵到胞外,从而导致肿瘤细胞产生耐药性。由于ABC跨膜转运蛋白超家族的这一特点,学者们开始致力于寻找能够有效抑制ABC跨膜转运蛋白家族的抑制剂。
近年来,一些酪氨酸激酶抑制剂如表皮生长因子受体抑制剂等被发现能够逆转ABC跨膜转运蛋白介导的多药耐药。Tivozanib(AV-951,KRN-951)是一种新型的酪氨酸激酶抑制剂,能够抑制血管内皮生长因子1、2、3。由于很多酪氨酸激酶抑制剂同时为ABCB1和ABCG2的逆转剂,本研究主要探索tivozanib与ABC跨膜转运蛋白之间的作用关系及其相关机制。
研究结果:
1.Tivozanib在浓度小于6μM时对于实验中所涉及的细胞株无明显细胞毒性。
2.Tivozanib在2.5μM和5μM的浓度时能够逆转ABCB1和ABCG2介导的多药耐药。MTT结果显示tivozanib在特定浓度能够显著降低耐药细胞株对于ABCB1转运底物紫杉醇、秋水仙碱和长春新碱的耐药性,以及ABCG2过表达细胞株对于ABCG2转运底物底物米托蒽醌、SN-38和多柔比星的耐药性。
3.Western blotting表明tivozanib抑制ABCB1、ABCG2的功能不是通过下调其蛋白表达来实现的。
4.Efflux assay和accumulation assay的结果证实tivozanib是通过抑制ABCB1和ABCG2转运蛋白的活性,进而增加细胞内化疗药物的积累来发挥逆转多药耐药的功能。
5.[125I]IAAP-photoaffinity labeling提示tivozanib能够与IAAP竞争与跨膜转运蛋白ABCB1、ABCG2的结合区域,说明tivozanib是通过直接结合于ABCB1、ABCG2转运蛋白的底物结合位点来发挥作用的。
6.ATPase试验表明tivozanib能够通过调节ABCB1和ABCG2结构域中ATP水解酶的活性,来抑制ABCB1和ABCG2介导的多药耐药。
结论:
1.Tivozanib在特定浓度能够逆转ABCB1、ABCG2跨膜转运蛋白介导的多药耐药。
2.Tivozanib逆转多药耐药的机制可能是通过直接与ABCB1、ABCG2蛋白的结构域相结合,调节ATP水解酶活性来实现的。
[1] Tivozanib is currently being evaluated in the pivotal Phase 3 TIVO-3 trial,a randomized,controlled,multi-center,open-label study to compare tivozanib to sorafenib in subjects with refractory advanced RCC.FDA approval is expected in 2018.A Study of Tivozanib(AV-951),an Oral VEGF Receptor Tyrosine Kinase Inhibitor,in the Treatment of Renal Cell Carcinoma,clinicaltrials.gov
[2] "AVEO Pharma surges 48%on recommendation for European approval of its cancer drug".Market Watch.June 28,2017.Retrieved June 28,2017.
[3] "Fotivda:EPAR–Product Information"(PDF).European Medicines Agency.2017-11-22.
[4] Campas,C.,Bolos,J.,Castaner,R(2009)."Tivozanib".Drugs Fut.34(10):793.
[5] Aveo Kidney Cancer Drug Shows Success;Shares Up,By John Kell,Dow Jones Newswires[dead link]
[6] "Phase III Results Lead Aveo and Astellas to Plan Regulatory Submissions for Tivozanib".3 Jan 2012.
[7] "Fotivda:EPAR–Public assessment report"(PDF).European Medicines Agency.2017-11-22.
[8] 阳丹雯.Tivozanib抑制ABCB1和ABCG2介导的肿瘤细胞多药耐药的相关研究[D].中南大学,2014.